|
Escuchar nota
Getting your Trinity Audio player ready...
|
…y otros 94 estudios relacionan el inóculo con miocarditis y pericarditis.
El Estudio se llama: 1 – «Anticuerpos IL-1RA en miocarditis después de la vacunación contra el SARS-CoV-2» y fue publicado el 21 de setiembre del 2022.

Fue presentado por los siguientes expertos:
Lorenz Thurner, M.D.
Saarland University, Homburg, Germany
lorenz.thurner@uks.eu
Christoph Kessel, Ph.D.
University Children’s Hospital Muenster, Muenster, Germany
Natalie Fadle
Evi Regitz
Saarland University, Homburg, Germany
Franziska Seidel, M.D.
German Heart Center Berlin, Berlin, Germany
Ingrid Kindermann, M.D.
Stefan Lohse, Ph.D.
Igor Kos, M.D.
Saarland University, Homburg, Germany
Carsten Tschöpe, M.D.
Charité University Medicine Berlin, Berlin, Germany
Parastoo Kheiroddin, M.Sc.
University Children’s Hospital Regensburg, Regensburg, Germany
Daniel Kiblboeck, M.D.
Johannes Kepler University, Linz, Austria
Marie-Christin Hoffmann
Birgit Bette
Gabi Carbon
Onur Cetin, M.D.
Klaus-Dieter Preuss, Ph.D.
Konstantinos Christofyllakis, M.D.
Joerg T. Bittenbring, M.D.
Saarland University, Homburg, Germany
Thomas Pickardt, M.D.
Competence Network for Congenital Heart Defects, Berlin, Germany
Yvan Fischer, Ph.D.
Rheinisch-Westfälische Technische Hochschule Aachen, Aachen, Germany
Holger Thiele, M.D.
Heart Center Leipzig, Leipzig, Germany
Stephan Baldus, M.D.
University Hospital Cologne, Cologne, Germany
Karl Stangl, M.D.
Charité University Medicine Berlin, Berlin, Germany
Stephan Steiner, M.D.
St. Vincenz Hospital, Limburg, Germany
Frank Gietzen, M.D.
Sebastian Kerber, M.D.
Thomas Deneke, M.D.
Cardiovascular Center Bad Neustadt–Saale, Bad Neustadt–Saale, Germany
Stefanie Jellinghaus, M.D.
Axel Linke, M.D.
Technische Universität Dresden, Dresden, Germany
Karim Ibrahim, M.D.
Klinikum Chemnitz, Chemnitz, Germany
Ulrich Grabmaier, M.D.
Steffen Massberg, M.D.
Ludwig-Maximilians-University, Munich, Germany
Christian Thilo, M.D.
RoMed Klinikum, Rosenheim, Germany
Simon Greulich, M.D.
Meinrad Gawaz, M.D.
University of Tübingen, Tübingen, Germany
Ertan Mayatepek, M.D.
University Children’s Hospital Duesseldorf, Duesseldorf, Germany
Lars Meyer-Dobkowitz, M.D.
Klinikum Westbrandenburg, Potsdam, Germany
Michael Kindermann, M.D.
CaritasKlinikum St. Theresia, Saarbrücken, Germany
Einat Birk, M.D.
Merav Birk, M.D.
Schneider Children’s Medical Center of Israel, Petach Tikva, Israel
Mitja Lainscak, M.D.
University of Ljubljana, Ljubljana, Slovenia
Dirk Foell, M.D.
University Children’s Hospital Muenster, Muenster, Germany
Philipp M. Lepper, M.D.
Robert Bals, M.D.
Marcin Krawczyk, M.D.
Saarland University, Homburg, Germany
Dror Mevorach, M.D.
Hadassah Medical Center, Jerusalem, Israel
Tal Hasin, M.D.
Shaare Zedek Medical Center, Jerusalem, Israel
Andre Keren, M.D.
Hadassah Hebrew University Hospital, Jerusalem, Israel
Michael Kabesch, M.D.
University Children’s Hospital Regensburg, Regensburg, Germany
Hashim Abdul-Khaliq, M.D.
Sigrun Smola, M.D.
Moritz Bewarder, M.D.
Saarland University, Homburg, Germany
Bernhard Thurner, M.D.
Klinikum Kempten, Kempten, Germany
Michael Böhm, M.D.
Jochen Pfeifer, M.D.
Saarland University, Homburg, Germany
Karin Klingel, M.D.
University Hospital Tübingen, Tübingen, Germany
El texto en español dice:
La miocarditis asociada con las vacunas de ARN mensajero (ARNm) contra el síndrome respiratorio agudo severo coronavirus 2 (SARS-CoV-2) afecta predominantemente a adolescentes varones y adultos jóvenes varones (14 a <30 años de edad) y generalmente ocurre después de recibir la segunda dosis de la vacuna. En adultos con enfermedad crítica por coronavirus 2019 (Covid-19) y en casos de síndrome inflamatorio multisistémico en niños (MIS-C), recientemente descubrimos autoanticuerpos neutralizantes dirigidos al antagonista del receptor de interleucina-1 endógeno (IL-1RA), que inhibe la señalización y la inflamación de la interleucina-1.
En este estudio, evaluamos la prevalencia de anticuerpos neutralizantes de IL-1RA y progranulina, que inhibe la señalización del factor de necrosis tumoral, en 69 pacientes (14 a 79 años de edad) con sospecha clínica de miocarditis después de la vacunación contra el SARS-CoV-2. Un total de 61 pacientes fueron sometidos a biopsia endomiocárdica.
La miocarditis se confirmó mediante biopsia en 40 de 61 pacientes (Figura 1A). Entre los pacientes con miocarditis confirmada histológicamente, se encontraron anticuerpos anti-IL-1RA en 9 de 12 pacientes (75 %) menores de 21 años, en comparación con 3 de 28 pacientes (11 %) de 21 años o más. Los anticuerpos anti-IL-1RA no fueron detectables en los 21 pacientes en los que la biopsia descartó el diagnóstico de miocarditis (Figura 1B y 1C). Los pacientes positivos para anticuerpos IL-1RA con miocarditis confirmada por biopsia tuvieron un inicio temprano de los síntomas, que ocurrió principalmente después de recibir la segunda dosis de la vacuna, y un curso más leve de miocarditis que los pacientes con miocarditis confirmada por biopsia pero sin anti-IL-1RA autoanticuerpos (Tablas S1 a S6 y Figs. S1 a S6 en el Apéndice complementario, disponible con el texto completo de esta carta en NEJM.org).
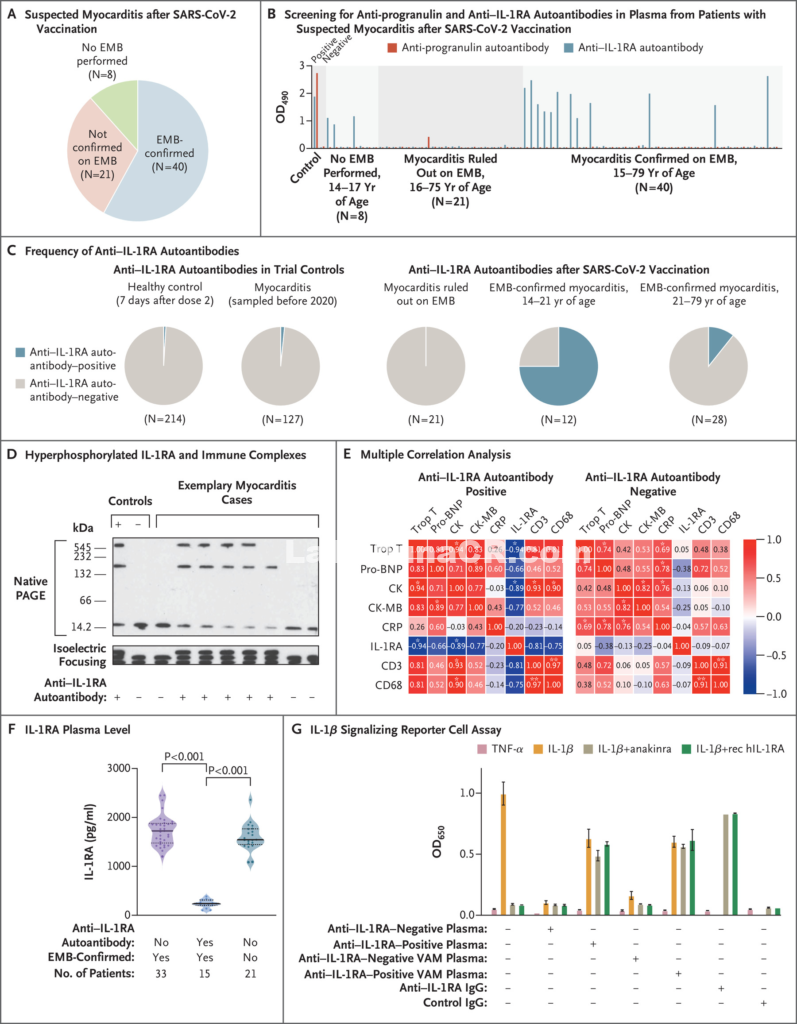
Se observaron anticuerpos IL-1RA en 2 de 214 participantes de control vacunados (1 %) y en 2 de 125 participantes (2 %) que tenían miocarditis comprobada histológicamente que se había diagnosticado antes de la pandemia de Covid-19.
Los datos anteriores que se habían obtenido de pacientes con covid-19 crítico no respaldaban la reactividad cruzada de los anticuerpos IL-1RA purificados con proteínas estructurales del SARS-CoV-2, incluida la proteína espiga,3 que argumenta en contra del virus o la vacuna. mimetismo molecular impulsado. La evidencia actual apunta hacia una hiperfosforilación transitoria de IL-1RA que precede a una ruptura de la tolerancia inmune periférica. o IgG)-proteína complejada con una isoforma atípica de IL-1RA ocurrió exclusivamente en pacientes que eran seropositivos para anticuerpos anti-IL-1RA (Figura 1D). Esta isoforma adicional de IL-1RA estaba hiperfosforilada en la posición 111 de treonina, lo que se había observado previamente en pacientes adultos con Covid-19 crítico y en pacientes con MIS-C.3,4 En contraste con nuestras observaciones en pacientes con miocarditis después del SARS-CoV -2, la IL-1RA no estaba hiperfosforilada en ninguna de las muestras que se habían obtenido de los participantes de control.
En el momento de la miocarditis aguda, el nivel plasmático medio (± DE) de IL-1RA libre en 15 pacientes seropositivos para anticuerpos anti–IL-1RA fue de 236±82 pg por mililitro, mientras que el nivel fue de 1736±312 pg por mililitro. en 33 pacientes sin anticuerpos anti-IL-1RA y 1599±277 pg por mililitro en 21 pacientes en los que el estudio histológico descartó el diagnóstico de miocarditis (Figura 1F). Los niveles plasmáticos de IL-1RA se correlacionaron con marcadores de daño cardíaco (troponina T, creatina cinasa, creatina cinasa MB o péptido natriurético tipo pro-B), infiltración en tejido cardíaco de células T CD3+ y macrófagos CD68+ e inflamación sistémica (C- proteína reactiva). Hubo una correlación negativa entre los marcadores de daño cardíaco y los niveles plasmáticos de IL-1RA en pacientes con anticuerpos anti-IL-1RA (Figura 1E). Los experimentos de ensayo del indicador de señalización de interleucina-1 mostraron un deterioro directo de la bioactividad de IL-1RA después de la adición de anticuerpos anti-IL-1RA del plasma de los pacientes (Figura 1G).
Nuestro estudio de la miocarditis asociada a la vacunación contra el SARS-CoV-2 y los anticuerpos anti-IL-1RA debe interpretarse en el contexto de que la transitoriedad de la hiperfosforilación (como se informó anteriormente en pacientes con Covid-19 crítico o MIS-C3,4) y los pacientes No se conocían los haplotipos HLA. En nuestro estudio, se observaron anticuerpos neutralizantes contra IL-1RA y una isoforma de IL-1RA hiperfosforilada en pacientes masculinos jóvenes con miocarditis confirmada por biopsia después de recibir la vacuna de ARNm de SARS-CoV-2. Estos anticuerpos afectaron la bioactividad de IL-1RA in vitro, se asociaron con niveles circulantes bajos de IL-1RA y se encontraron en pacientes con evidencia de biomarcadores de daño cardíaco e inflamación.
PARA IR A LA FUENTE ORIGINAL: https://www.nejm.org/doi/full/10.1056/NEJMc2205667
Juramento de Hipócrates: Y NO DARÉ NINGUNA DROGA LETAL A NADIE, AUNQUE ME LA PIDAN, NI SUGERIRÉ SU USO.
EXISTEN INFINIDAD DE ESTUDIOS QUE ALERTAN SOBRE LA PERICARDITIS Y MIOCARDITIS COMO CONSECUENCIA DE LA VACUNA COVID, AQUI LES DEJAMOS LOS MAS IMPORTANTES:
2 – Miocarditis y pericarditis después de la vacunación con ARNm de COVID-19:consideraciones prácticas para los proveedores de atención https://www.sciencedirect.com/science/article/pii/S0828282X21006243300
3 – Miocarditis con vacunas COVID-19 ARNm https://www.ahajournals.org/doi/pdf/10.1161/CIRCULATIONAHA.121.056135301
4 – Miocarditis y otras complicaciones cardiovascularesde las vacunas COVID-19 basadas en ARNm https://pubmed.ncbi.nlm.nih.gov/34277198/302
5 -Pericarditis tras la administración de la vacunaCOVID-19 ARNm BNT162b2 https://pubmed.ncbi.nlm.nih.gov/34364831/303
6 – Presentación inusual de perimiocarditis agudadespués de la vacunación contra el SARS-COV-2 mRNA-1237 Moderna https://pubmed.ncbi.nlm.nih.gov/34447639/304
7 – Miocarditis aguda tras la segunda dosis de lavacuna mRNA-1273 SARS-CoV-2 https://pubmed.ncbi.nlm.nih.gov/34514306/305
8 – Miocarditis aguda tras la administración de la vacuna BNT162b2 frente a COVID-19 https://www.sciencedirect.com/science/article/abs/pii/S188558572100133X306
9 – Hallazgos de resonancia magnética cardiovascular en pacientes adultos jóvenes con miocarditis aguda tras la vacunación con ARNm COVID-19 https://pubmed.ncbi.nlm.nih.gov/34496880/307
10 – Perimiocarditis después de la vacunación con COVID-19 https://pubmed.ncbi.nlm.nih.gov/34866957/308
11 – Epidemiología de la miocarditis / pericarditis aguda en adolescentes de Hong Kong después de la vacunación COVID-19 https://pubmed.ncbi.nlm.nih.gov/34849657/309
12 – Muerte súbita inducida por miocarditis despuésde la vacunación con ARNm deBNT162b2 COVID-19 en Corea: informe de caso que se centra en los hallazgos histopatológicos https://pubmed.ncbi.nlm.nih.gov/34664804/310
13 – Miocarditis aguda después de la vacunación conARNm de COVID-19 en adultos de 18 años o más https://pubmed.ncbi.nlm.nih.gov/34605853/311
14 – Varón joven con miocarditis después de la vacunacióncon ARNm-1273 contra la enfermedad por coronavirus-2019 COVID-19 https://pubmed.ncbi.nlm.nih.gov/34744118/312
15 – Miocarditis aguda después de la vacunación contrael SARS-CoV-2 en un hombre de 24 años https://pubmed.ncbi.nlm.nih.gov/34334935/313
16 – Miocarditis tras la vacunación con ARNm contrael SARS-CoV-2, una serie de casos https://www.sciencedirect.com/science/article/pii/S2666602221000409314
17 – Miocarditis y pericarditis después de la vacunación contra COVID-19 https://jamanetwork.com/journals/jama/fullarticle/2782900315 –
18 – Miocarditis asociada con vacunación COVID-19 https://www.ahajournals.org/doi/pdf/10.1161/CIRCULATIONAHA.121.055891316
19 – Miocarditis aguda tras la administración dela vacuna BNT162b2 contra COVID-19 https://pubmed.ncbi.nlm.nih.gov/33994339/317
20 – Asociación entre la vacuna COVID-19 Ad26.COV2.S y la miocarditis aguda: reporte de un caso y revisión de la literatura https://www.sciencedirect.com/science/article/pii/S1553838921005789318
21 – Miocarditis inducida por la vacuna COVID-19: reporte de un caso con revisión de la literatura https://www.sciencedirect.com/science/article/pii/S1871402121002253319
22 – Posible asociación entre la vacuna COVID-19y la miocarditis: hallazgos clínicos y deRMC https://www.sciencedirect.com/science/article/pii/S1936878X2100485X320
23 – Vacunación de ARNm COVID-19 y desarrollo demiopericarditis confirmada por CMR https://www.medrxiv.org/content/10.1101/2021.09.13.21262182v1.full?s=09321
24 – Miocarditis fulminante e hiperinflamación sistémica asociada a la vacunación conARNm de BNT162b2 COVID-19 https://www.sciencedirect.com/science/article/pii/S0167527321012286322
25 – Miocarditis aguda tras la administración dela vacuna BNT162b2 https://www.sciencedirect.com/science/article/pii/S2214250921001530323
26 – Miocarditis tras la vacunación con BNT162b2 en un varón sano https://www.sciencedirect.com/science/article/pii/S0735675721005362324
27 – Miocarditis aguda después de la vacunación Comirnaty (Pfizer) en un hombre sano con infección previa por SARS-CoV-2 https://www.sciencedirect.com/science/article/pii/S1930043321005549325 –
28 – Pericarditis tras la administración de la vacuna de ARNm BNT162b2 contra laCOVID-19 https://www.sciencedirect.com/science/article/pii/S1885585721002218326
29 – Miocarditis aguda después de la vacunación conARNm-1273 SARS-CoV-2 https://www.sciencedirect.com/science/article/pii/S2589790X21001931327
30 – Relación entre la segunda dosis de la vacuna Covid-19 de ARNm de BNT162b2 y la afectación cardíaca en un paciente con infección previa por SARS-COV-2 https://www.sciencedirect.com/science/article/pii/S2352906721000622328
31 – Miocarditis aguda después de la vacunación contraSARS-CoV-2 https://www.sciencedirect.com/science/article/pii/S0870255121003243329
32 – Una serie de pacientes con miocarditis después de la vacunación contra elSARS-CoV-2 con mRNA-1279 y BNT162b2 https://www.sciencedirect.com/science/article/pii/S1936878X21004861330
33 – Vacuna de ARNm de COVID-19 y miocarditis https://pubmed.ncbi.nlm.nih.gov/34268277/331
34 – Miocarditis con vacunas covid-19 ARNm https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.121.056135332
35 – Vacuna COVID-19 y miocarditis https://pubmed.ncbi.nlm.nih.gov/34399967/333
36 – Miocarditis y vacunas COVID-19 https://pubmed.ncbi.nlm.nih.gov/34246566/334
37 – Miocarditis, pericarditis y miocardiopatía después de la vacunación COVID-19 https://pubmed.ncbi.nlm.nih.gov/34340927/335
38 – Miocarditis que se presenta después de la inmunizacióncon vacunas COVID-19 basadas en ARNm https://jamanetwork.com/journals/jamacardiology/fullarticle/2781600100.336
39 – Pacientes con miocarditis aguda después de la vacunación con ARNm COVID-19 https://jamanetwork.com/journals/jamacardiology/fullarticle/2781602337
40 – Miocarditis asociada a la vacunación con ARNmCOVID-19 https://pubs.rsna.org/doi/10.1148/radiol.2021211430338
41 – La inyección intravenosa de la vacuna de ARNm de la enfermedad del coronavirus 2019 (COVID-19) puede inducir la miopericarditis aguda https://t.co/j0IEM8cMXI339
42 – Un informe sobre eventos adversos de miocarditis en el sistema de notificación de eventos adversos de vacunas de EE. UU. (VAERS) en asociación con productos biológicos inyectables COVID-19 https://pubmed.ncbi.nlm.nih.gov/34601006/340
43 – Riesgo excesivo de miocarditis tras la vacunaCOVID-19 https://www.nejm.org/doi/full/10.1056/NEJMoa2110475?query=featured_home341
44 – Las vacunas mARN COVID aumentan drásticamentelos marcadores inflamatorios endoteliales y el riesgo de Síndrome Coronario Agudo medido por la prueba cardíacaPULS: una advertencia https://www.ahajournals.org/doi/10.1161/circ.144.suppl_1.10712342
45 – Hallazgos de resonancia magnética cardiovascular en pacientes adultos jóvenes con miocarditis aguda tras la vacunación con ARNm COVID-19: una serie de casos https://jcmr-online.biomedcentral.com/articles/10.1186/s12968-021-00795-4343
46 – Imágenes cardíacas de miocarditis aguda después de la vacunación con ARNm de COVID-19 https://pubmed.ncbi.nlm.nih.gov/34402228/344
47 – Reporte de caso: miocarditis aguda tras la segunda dosis de la vacuna mRNA-1273SARS-CoV-2 https://academic.oup.com/ehjcr/article/5/8/ytab319/6339567345
48 – Miocarditis / pericarditis asociada a la vacuna COVID-19 https://science.gc.ca/eic/site/063.nsf/eng/h_98291.html109346
50 – La nueva plataforma de vacunas de ARNm COVID-19 y miocarditis: pistas sobre el posible mecanismo subyacente https://pubmed.ncbi.nlm.nih.gov/34312010/347
51 – Lesión aguda del miocardio después de la vacunación COVID-19: informe de un caso y revisión de la evidencia actual de la base de datos del sistema de notificación de eventos adversos de las vacunas https://pubmed.ncbi.nlm.nih.gov/34219532/348
52 – Esté alerta al riesgo de eventos cardiovasculares adversos después de la vacunación COVID-19 https://www.xiahepublishing.com/m/2472-0712/ERHM-2021-00033349
53 – Miocarditis asociada con la vacunación COVID-19: hallazgos de ecocardiografía,tomografía cardíaca y resonancia magnética https://www.ahajournals.org/doi/10.1161/CIRCIMAGING.121.013236350
54 – Evaluación en profundidad de un caso de miocarditis después de la segunda dosis de la vacuna de ARNm de COVID-19 https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.121.056038351
55 – Aparición de miocarditis aguda similar a un infarto tras la vacunación con COVID-19: ¿solo una coincidencia accidental o más bien una miocarditis autoinmune asociada a la vacunación? https://pubmed.ncbi.nlm.nih.gov/34333695/352
56 – Miocarditis después de la vacunación contra el SARS-CoV-2: ¿una reacción inducida por la vacuna? https://pubmed.ncbi.nlm.nih.gov/34118375/353 –
57 – Miocarditis, pericarditis y miocardiopatía después de la vacunación COVID-19 https://www.sciencedirect.com/science/article/pii/S1443950621011562354
58 – Perimiocarditis aguda después de la primera dosis de la vacuna de ARNm contra COVID-19 https://pubmed.ncbi.nlm.nih.gov/34515024/355
59 – Presentación inusual de perimiocarditis aguda después de la vacunación moderna con ARNm-1237 del SARS-COV-2 https://pubmed.ncbi.nlm.nih.gov/34447639/356
60 – Perimiocarditis después de la primera dosis de la vacuna mRNA-1273 SARS-CoV-2 (Moderna) en un varón joven sano https://bmccardiovascdisord.biomedcentral.com/articles/10.1186/s12872-021-02183-3357
61 – Miocarditis aguda después de la segunda dosis de la vacuna SARS-CoV-2: ¿Relación causal? https://pubmed.ncbi.nlm.nih.gov/34236331/358
62 – Miocarditis después de la inmunización con vacunasde ARNm COVID-19 en miembros del ejército de EEUU. Reporte de 23 pacientes masculinos, incluidos 22 militares previamente sanos, se identificó miocarditis dentro de los 4 días posteriores a la recepción de la vacuna https://jamanetwork.com/journals/jamacardiology/fullarticle/2781601359
63 – 68 Imágenes de PET digital con Ga-DOTATOC de infiltrados de células inflamatorias en miocarditis después de la vacunación con COVID-19 https://pubmed.ncbi.nlm.nih.gov/34746968/360
64 – Miocarditis tras la vacunación con ARNm contra el SARS-CoV-2, una serie de casos https://pubmed.ncbi.nlm.nih.gov/34396358/361
65 – Aparición de miocarditis aguda similar a un infarto después de la vacunación conCOVID-19: ¿solo una coincidencia accidental o más bien una miocarditis autoinmune asociada a la vacunación? https://pubmed.ncbi.nlm.nih.gov/34333695/362
66 – Epidemiología de la miocarditis y la pericarditis después de las vacunas de ARNm en Ontario, Canadá: por producto de vacuna, programa e intervalo https://www.medrxiv.org/content/10.1101/2021.12.02.21267156v1363
67 – Infarto agudo de miocardio y miocarditis después de la vacunación COVID-19 https://pubmed.ncbi.nlm.nih.gov/34586408/364
68 – Infarto agudo de miocardio dentro de las 24 horas posteriores a la vacunación COVID-19 https://pubmed.ncbi.nlm.nih.gov/34364657/365
69 – Miocarditis después de la inmunización con vacunas de ARNm COVID-19 en miembros del ejército de USA https://pubmed.ncbi.nlm.nih.gov/34185045/366
70 – Miocarditis tras la vacunación con BNT162b2 en un varón sano https://pubmed.ncbi.nlm.nih.gov/34229940/367
71 – Miocarditis aguda después de la vacunación conARNm-1273 SARS-CoV-2 https://pubmed.ncbi.nlm.nih.gov/34308326/368 –
72 – Dolor en el pecho con nuevo desarrollo anormal de electrocardiograma después de la inyección de la vacuna COVID-19 fabricada por Moderna https://pubmed.ncbi.nlm.nih.gov/34866106/369
73 – Un caso de encefalopatía aguda e infarto demiocardio sin elevación del segmento STtras la vacunación con ARNm-1273: ¿posible efecto adverso? https://pubmed.ncbi.nlm.nih.gov/34703815/370
74 – Informe de un caso de miopericarditis después de la vacunación con ARNm deBNT162b2 COVID-19 en un varón joven coreano https://pubmed.ncbi.nlm.nih.gov/34636504/371
75 – Miocarditis aguda después de la vacunación COVID-19 https://docs.google.com/document/d/1Hc4bh_qNbZ7UVm5BLxkRdMPnnI9zcCsl/e372
76 – Miocarditis aguda después de la vacunación Comirnaty en un hombre sano https://pubmed.ncbi.nlm.nih.gov/34367386/373
77 – Miocardiopatía de Takotsubo tras vacunación por coronavirus 2019 en paciente en hemodiálisis de mantenimiento https://pubmed.ncbi.nlm.nih.gov/34731486/374
78 – Miocardiopatía de Takotsubo después de la vacunacióncon ARNm COVID-19 https://www.sciencedirect.com/science/article/pii/S1443950621011331375
79 – Miocardiopatía de Takotsubo después de la vacunación con ChAdOx1 nCoV-19 https://pubmed.ncbi.nlm.nih.gov/34625447/376
80 – Síndrome de Takotsubo después de recibir la vacuna COVID-19 https://pubmed.ncbi.nlm.nih.gov/34539938/377
81 – Síndrome coronario agudo de Kounis tipo 1 inducido por la vacuna inactivada contra el SARS-COV-2 https://pubmed.ncbi.nlm.nih.gov/34148772/378
82 – Infarto agudo de miocardio dentro de las 24 horas posteriores a la vacunación COVID-19 ¿Es el síndrome de Kounis el culpable? https://pubmed.ncbi.nlm.nih.gov/34702550/379
83 – Infarto prematuro de miocardio o efecto secundariode la vacuna COVID-19 https://pubmed.ncbi.nlm.nih.gov/33824804/380
84 – Infarto de miocardio, accidente cerebrovascular y embolia pulmonar después de la vacuna COVID-19 de ARNm de BNT162b2 en personas de 75 años o más https://pubmed.ncbi.nlm.nih.gov/34807248/381
85 – Miocarditis fulminante aguda y shock cardiogénico después de la vacunación por coronavirus de ARN mensajero en 2019 que requirió reanimación cardiopulmonar extracorpórea https://pubmed.ncbi.nlm.nih.gov/34778411/382
86 – Imagen multimodal e histopatología en un joven que presenta miocarditis linfocítica fulminante y shock cardiogénico después de la vacunación con ARNm-1273 https://pubmed.ncbi.nlm.nih.gov/34848416/383
87 – Infarto de miocardio y trombosis de las venas ácigos tras la vacunación con ChAdOx1nCoV-19 en un paciente en hemodiálisis https://pubmed.ncbi.nlm.nih.gov/34650896/384
88 – Miocarditis aguda después de la vacunación contrala enfermedad por coronavirus 2019 https://pubmed.ncbi.nlm.nih.gov/34734821/385
89 – Una serie de pacientes con miocarditis despuésde la vacunación contra elSARS-CoV-2 con mRNA-1279 y BNT162b2 https://pubmed.ncbi.nlm.nih.gov/34246585/386 –
90 – Miopericarditis después de la vacuna contrala enfermedad del coronavirus de ácido ribonucleico mensajero de Pfizer en adolescentes https://pubmed.ncbi.nlm.nih.gov/34228985/387
91 – Miocarditis aguda definida después de la vacunación con ARNm 2019 de la enfermedad por coronavirus https://pubmed.ncbi.nlm.nih.gov/34866122/388
92 – Disfunción sistólica biventricular en miocarditis aguda después de la vacunación SARS-CoV-2 mRNA-1273 https://pubmed.ncbi.nlm.nih.gov/34601566/389
93 – Miocarditis tras vacunación COVID-19: estudio de resonancia magnética https://pubmed.ncbi.nlm.nih.gov/34739045/390
94 – Miocarditis aguda en un adulto joven dos días después de la vacunación con Pfizer https://pubmed.ncbi.nlm.nih.gov/34709227/391
95 – Miocarditis tras la vacunación con Covid-19 en una gran organización sanitaria https://pubmed.ncbi.nlm.nih.gov/34614329/
Queremos presentarles al Dr. Robert Malone

La experiencia del Dr. Malone abarca desde la investigación básica hasta el desarrollo (clínico) avanzado. Es especialista en asuntos médicos así como en asuntos regulatorios. Esto incluye escribir, desarrollar, revisar y administrar ensayos clínicos de vacunas, bioamenazas y productos biológicos y estrategias de desarrollo clínico. Ha estado involucrado en el desarrollo, diseño y supervisión de aproximadamente en cuarenta ensayos clínicos de fase 1 y veinte ensayos clínicos de fase 2, así como cinco ensayos clínicos de fase 3 y fue el inventor de la técnica ARNm que se está probando actualmente con las vacunas covid.
Se ha desempeñado como director médico/monitor médico en aproximadamente cuarenta ensayos clínicos de fase 1 y en veinte ensayos clínicos de fase 2, incluidos los realizados en organizaciones de investigación clínica centradas en vacunas.
Se ha desempeñado como investigador principal en algunos de estos. El Dr. Malone tiene una amplia experiencia en investigación y desarrollo en las áreas de investigación de descubrimiento preclínico, ensayos clínicos, vacunas, terapia génica, biodefensa (desarrollo de contramedidas médicas) e inmunología.
Tiene más de veinte años de experiencia en gestión y liderazgo en la industria académica, farmacéutica y biotecnológica, así como en organizaciones gubernamentales y no gubernamentales. Formado científicamente en UC Davis, UC San Diego y en los laboratorios de Biología Molecular y Virología del Instituto Salk, el Dr. Malone es un científico reconocido internacionalmente (virología, inmunología, biología molecular) y es uno de los inventores originales de la «vacunación con ADN».
Entrega de ARNm (ARN como fármaco) y entrega in vivo de ácidos nucleicos usando lípidos catiónicos y campos eléctricos pulsados. El Dr. Malone posee numerosas patentes nacionales y extranjeras fundamentales en los campos de administración de genes, formulaciones de administración y vacunas.
El Dr. Malone tiene 11.060 citas de sus publicaciones, según lo verificado por Google Scholars. Recibió su formación médica en la Universidad Northwestern (MD) y la Escuela de Medicina de la Universidad de Harvard (Postgrado en Investigación Clínica), y en Patología en UC Davis. Se ha desempeñado como Profesor Asistente de Patología en el Centro Médico UC Davis/Sacramento y en la Facultad de Medicina de la Universidad de Maryland, y como Profesor Asociado de Cirugía en la Universidad Uniformada de Ciencias de la Salud. Tiene más de 75 publicaciones revisadas por pares y ha sido orador invitado y presidente de más de 40 conferencias. Pondría UD. en duda lo que éste científico puede aportar al tema???
Aunque nada de ésto lo informa la prensa tradicional en Costa Rica, es importante que vean como se habla de éste tema en medios internacionales:
NOTA EDITORIAL:
NOS PREGUNTAMOS, en que mundo viven médicos, enfermeras y personal sanitario en general que no se han enterado de toda ésta literatura médica??? O acaso es que la pregunta debería ser otra: Qué clase de médicos, enfermeras y personal de salud son los que tenemos trabajando en todo el sistema de salud tanto público como privado que ignoran toda ésta evidencia científica???
Y claro, definitivamente debemos preguntarnos: que clase de médicos integran la Comisión Nacional de Vacunación y Epidemiología, y que clase de médico es la Dra. Joselyn Chacón, que preside dicha comisión y además es la máxima autoridad en materia de salud si se hacen de la vista gorda ante todo ésto???
Y por supuesto: Que clase de médicos son esos que dirigen el Colegio de Médicos que no han alzado la voz y alertado de todos éstos estudios???
Y por último, si usted leyó éste artículo, le pregunto: va a seguir exponiéndose a todo éste riesgo y va a exponer a sus hijos a éste peligro???


La CCSS, ministerio de salud, la CNVE mienten al público al no informar correctamente mediante el consentimiento informado que las «vkns» COVID-19 poseen graves efectos adversos, por esa razón, no desean un debate científico sobre el tema y mediante la coacción e imposición de los más totalitarios gobiernos obligan a vacunarse a las personas.
#el_contrato_no_es_secreto_de_estado
#el_contrato_pfizer_debe_ser_público