|
Escuchar nota
Getting your Trinity Audio player ready...
|
El descubrimiento y desarrollo de nuevos fármacos es un proceso largo, normalmente transcurren entre diez y quince años desde la investigación inicial hasta el lanzamiento de un medicamento al mercado, incluidos los -entre seis y ocho años- que transcurren entre los ensayos clínicos de Fase I y el lanzamiento al mercado.

Descubrimiento y desarrollo de fármacos
Con el desarrollo de la industria farmacéutica a finales del siglo XIX, el descubrimiento de fármacos se convirtió en un proceso sumamente orientado y gestionado y dejó de ser el terreno de médicos para pasar al terreno de científicos contratados para este propósito. La mayor parte de la terapéutica y la farmacología modernas se basa en fármacos procedentes de los laboratorios de estas compañías farmacéuticas, sin los cuales la práctica de la terapéutica y la ciencia de la farmacología no serían más que un pequeño fragmento de lo que han llegado a ser en la actualidad.
Tal y como señala la última edición de Rang y Dale. Farmacología, en general, el proceso puede dividirse en tres fases principales antes de su comercialización:
- Descubrimiento del fármaco, o fase en la que se eligen las moléculas candidatas en función de sus propiedades farmacológicas. (duración de 2 a 5 años)
- Desarrollo preclínico, o fase en la que se realiza un amplio abanico de estudios en seres no humanos (p. ej., pruebas de toxicidad, análisis farmacocinético/farmacodinámico y formulación). (duración de 1 a 5 años)
- Desarrollo clínico, o fase en la que se prueba la eficacia, los efectos secundarios y los peligros potenciales que el fármaco seleccionado provoca en voluntarios sanos y en pacientes. (duración de 5 a 7 años)
Esas tres fases, se consideran fases experimentales porque se llevan a cabo sin que cuenten con la aprobación para su comercialización por parte de las autoridades reguladoras, FDA (EEUU) y EMA (Europa).
Concluidas esas tres fases experimentales, se pasa a la solicitud de aprobación para que el producto sea aprobado, cuente con los registros sanitarios y pueda ser comercializado. (duración de 1 a 2 años)
4. Vigilancia tras la comercialización, o fase 4 es la vigilancia constante que deben hacer los fabricantes y las autoridades sanitarias tras la salida al mercado de un nuevo fármaco, monitoreando efectos adversos y resultados terapéuticos.
Muchas personas han afirmado que las actuales vacunas contra la covid 19 son experimentales por estar en fase 3, por no contar con registros sanitarios, por ser una técnica nunca antes utilizada (ARNm), por ser administrada únicamente con una «autorización de uso de emergencia», etc.
¿Qué es una Autorización de Uso de Emergencia (EUA, por sus siglas en inglés)?
Una Autorización de Uso de Emergencia (EUA, por sus siglas en inglés), es un mecanismo para facilitar la disponibilidad y el uso de contramedidas médicas, incluidas las vacunas, durante las emergencias de salud pública, como la actual pandemia causada por el COVID-19. En virtud de una EUA, la FDA puede permitir el uso de productos médicos no aprobados, o los usos no aprobados de productos médicos aprobados en una emergencia para diagnosticar, tratar o prevenir enfermedades o afecciones graves o que pongan en peligro la vida, cuando se hayan cumplido ciertos criterios regulatorios, entre ellos que no existan alternativas adecuadas, aprobadas y disponibles. (fuente: FDA)
Como se ve, el único requisito para que un medicamento NO PROBADO reciba una Autorización de Uso de Emergencia es que no existan alternativas para tratar una enfermedad, y eso explica sin lugar a dudas la razón por la que otras terápias como la Hidroxicloroquina, la Ivermectina, el dióxido de cloro o la Plata Coloidal fueron prohibidos, desacreditados y hasta satanizados.
ES ESO CIERTO???
Muchas veces oímos al ex ministro Daniel Salas decir que eso es falso, lo mismo los fact checkers, muy especialmente a #NoComaCuento de la nación decir que las vacunas no están en fase experimental.
En el siguiente documento correspondiente al acta de la sesión extraordinaria # XLI-2021 con fecha 24 de agosto del 2021 de la CNVE, el Dr. Porras explica que la vacuna si está en fase 3.

En una web del gobierno español, están los prospectos de todas las vacunas disponibles:
Ingresar a la web: CLICK AQUÍ

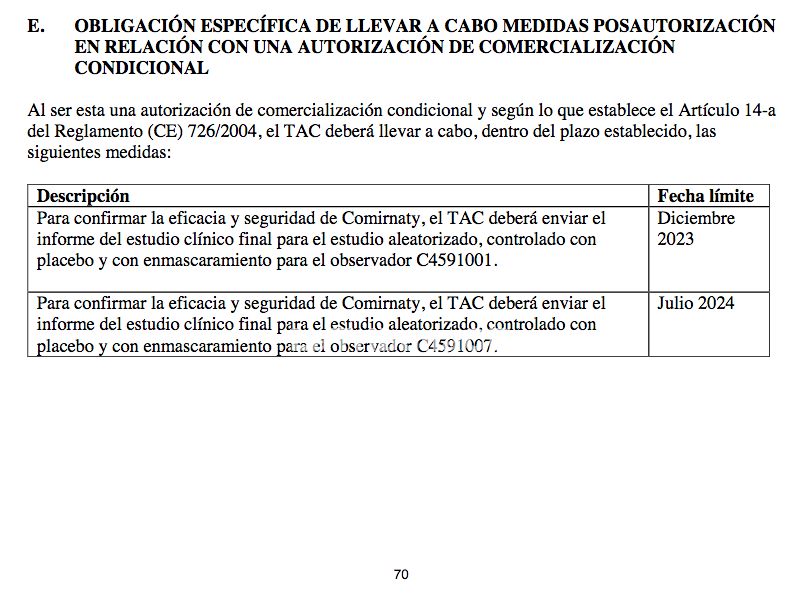
Al ingresar al prospecto de la vacuna Comirnaty de Pfizer/BioNTech, en la página 70 se lee:
Para confirmar la eficacia y seguridad de Comirnaty, el TAC deberá enviar el informe del estudio clínico final para el estudio aleatorizado, controlado con placebo y con enmascaramiento para el observador C4591001 a más tardar en diciembre del 2023.
Para confirmar la eficacia y seguridad de Comirnaty, el TAC deberá enviar el informe del estudio clínico final para el estudio aleatorizado, controlado con placebo y con enmascaramiento para el observador C4591007 a más tardar en julio del 2024.
Desde nuestro entender, no cabe ninguna duda que la vacuna si está en Fase 3, que es una fase experimental donde los fabricantes realizan estudios en VOLUNTARIOS, algo que no se ha hecho y es la razón por lo que en Costa Rica no se dió lo del consentimiento informado, sino que SE MINTIÓ sobre ese hecho, y se emitió una obligatoriedad que es algo antagónico al consentimiento libre e informado.
Otro hecho que también es innegable, es que Pfizer modificó las fechas de vencimiento cuando su producto se había distribuido con fechas próximas a su vencimiento, por eso le «extendieron su vida útil», un procedimiento totalmente irregular en el tema de los productos farmacéuticos. Esto consta en un documento llamado: HOJA INFORMATIVA PARA PROVEEDORES DE LA SALUD QUE ADMINISTREN LA VACUNA (páginas 4 y 5)
Cajas y viales de la vacuna COVID-19 de Pfizer-BioNTech suministrados en viales multidosis con tapa morada con fecha de caducidadde octubre de 2021 a diciembre de 2022 impresos en la etiqueta pueden permanecer en uso despuésde la fecha impresa hasta la fecha de caducidad que se muestra a continuación; mientras se hayan mantenido las condiciones de almacenamiento aprobadas.
Fecha de caducidad impresa Fecha de caducidad actualizada
12/2021→ 30-Jun-2022
01/2022→ 31-Jul-2022
02/2022→ 31-Ago-2022
03/2022→ 30-Sep-2022
06/2022→ 30-Sep-2022
07/2022→ 31-Oct-2022
08/2022→ 30-Nov-2022
09/2022→ 31-Dic-2022
10/2022→ 31-Ene-2023
11/2022→ 28-Feb-2023
12/2022→ 31-Mar-2023
VER DOCUMENTO: HAGA CLICK AQUÍ
SOBRE LOS CONTRATOS.
Otra de las anomalías que continuan bajo un manto de misterio son los contratos que ésta compañía OBLIGO a firmar a los países adquirientes, en un momento donde reinaba el pánico y dónde todos los países creían que la vacuna era la solución a la pandemia. El contrato con la Unión Europea dice:
Que toda la responsabilidad queda en manos de la Comisión Europea y de los países miembros. La farmacéutica se responsabiliza de algún fallo que pudiera registrarse en la fabricación del suero, pero a partir de la entrega del mismo a los países miembros, la multinacional no se responsabiliza, ni afrontará ninguna indemnización. (fuente: La Vanguardia)
Es la primera vez que un fabricante de un medicamente se blinda contra demandas por la fabricación de uno de sus productos, traslando la responsabilidad a los compradores. Eso es algo similar a que Coca Cola no pueda ser demandada si por el consumo de uno de sus productos resultase intoxicado un gran número de personas y los afectados solo pudieran demandar al pulpero que las vendió. El pulpero no tiene forma posible para saber que un producto que le compra a una trasnacional como Coca Cola distribuyó un producto en mal estado y por eso no puede cargar con esa responsabilidad…, de igual forma, un país comprador de esas vacunas, no tiene por qué saber lo que contienen los viales de vacunas, por lo tanto el único responsable por daños provocados por una sustancia farmacéutica, debe ser el fabricante.
Sólo imaginen si Pfizer y los otros fabricantes, tuvieran que afrontar las demandas de todas éstas personas:

Fuente de muertes y reacciones adversas: HAGA CLICK AQUÍ
Algunas noticias que deberías leer sobre Tedros Adhanom, director de la Organización Mundial de la Salud OMS
https://www.elcorreo.com/sociedad/salud/tedros-adhanom-viajero-20200426182711-ntrc.html


[…] LEA AQUÍ: LAS FASES DE UN MEDICAMENTO […]
[…] LE PUEDE INTERESAR: LAS FASES DE UN MEDICAMENTO […]